
 | |
|
Главная » Публицистика 0 ... 108 109 110 111 112 113 114 ... 159 На рис. V.62 показан план блока фильтровальной станции (совмещенной с насосной станцией второго подъема) и реагентного хозяйства. На рисунке показаны только основные линии труб, обозначенные теми же буквами, что и на рис. V.61. Кроме того, показана напорная линия промывной воды. Лаборатории и помещения обслуживающего персонала размещены на втором этаже в правой части здания (на рисунке не показаны). На рис. V.63 показан план расположения отстойников и камер хлопьеобразования (блок 6 на рис. V.61). Линии труб обозначены теми же буквами, что и на рис. V. 61. На рис. V.64 показан генеральный план крупной очистной станции производительностью 100 тыс. мсутки (проект Гипрокоммунводо-канала). Здесь/ - блок горизонтальных отстойников и фильтров с примыкающим к нему блоком служебных помещений 2. Реагентное хозяйство расположено в отдельном здании 3. На плане показаны места расположения пескового хозяйства 4, расходный склад хлора 5, сооружения для обработки промывной воды (для ее повторного использования) 6. На той же площадке располагаются резервуары чистой воды 7 и насосная станция второго подъема 8. В последних проектах станций осветления и обеззараживания 1 Впроп канализацию 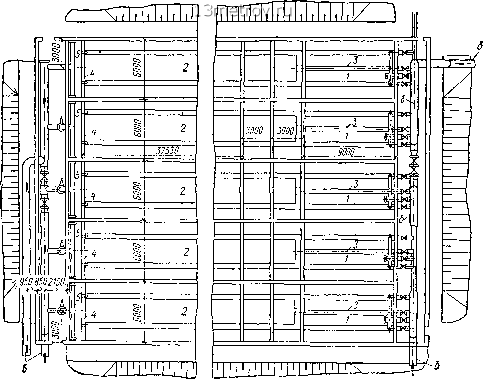 Рис V63 / - камеры хлопьеобразования; 2 - отстойники; 3 - сбросные трубы; 4 - дырчатая перегородка 5 - сборные дырчатые трубы 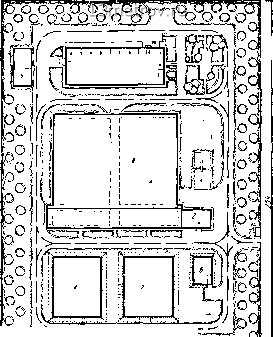 Рис. V 64 ВОДЫ ДЛЯ устройства сооружений широко применяется сборный железобетон, при проектировании зданий станций используется стандартная сетка пролетов, принятая в промышленном строительстве. Глава 23 УМЯГЧЕНИЕ, ОБЕССОЛИВАНИЕ И ОПРЕСНЕНИЕ ВОДЫ Умягчение воды - процесс понижения ее жесткости, обусловленной наличием солей кальция и магния. Существует несколько методов снижения жесткости воды, выбор которых производится исходя из требований к качеству умягчаемой воды (глубины умягчения) и технико-экономических обоснований. В практике водоподготовки наибольшее распространение получили следующие методы умягчения воды: а) реагентный, сущность которого заключается в связывании ионов кальция и магния химическими веществами в малорастворимые и легко удаляемые соединения - карбонат кальция и гидроокись магния (часто реагентный метод умягчения воды называют методом осаждения); в зависимости от применяемого реагента различают известковый, содовый, едконатриевый и фосфатный способы реагентного умягчения воды; б) катионитный, основанный на способности ионообменных мате- риалов (в данном случае катионитов) обменивать присутствующие в воде катионы кальция и магния на обменные катионы натрия или водорода (не придающие воде свойства жесткости), которыми предварительно заряжается катионит; обмен ионов натрия называется Na-кати-онированием, а ионов водорода - Н-катионированием; в) термохимический, при котором реагентное умягчение осуществляют обычно с применением извести и соды или реже едкого натра и соды при температуре воды более 100° С (до 165° С). Термохимический метод умягчения применяется в основном при подготовке воды для питания котлов. Только в этом случае утилизируется почти все тепло, затраченное на подогрев воды. Глубина умягчения известкованием определяется растворимостью карбоната кальция и гидроокиси магния; при совместном присутствии в воде кальция и магния теоретически глубина умягчения при температуре 0° С составляет 0,55 мг-экв/л, а при температуре 80° С- 0,23 мг-экв/л. Практически вода, умягченная известковым или известко-во-содовым способом, имеет остаточную жесткость не менее 0,5- 1 мг-экв/л из-за способности карбоната кальция и гидрата окиси магния образовывать пересыщенные растворы. § 122. ОСНОВЫ РЕАГЕНТНОГО УМЯГЧЕНИЯ ВОДЫ Способы реагентного умягчения воды перечислены в табл. V.11.
Применяется обычно после известково содового умягчения Применение ограничивается дефицитностью и высокой стоимостью бариевых солей Известковый способ (декарбонизацию воды) применяют, когда необходимо снизить щелочность исходной воды. При этом происходит эквивалентное снижение жесткости. При введении в воду гидрата окиси кальция сначала происходит связывание растворенной в воде углекислоты с образованием бикарбонатных ионов. Затем бикарбонатные ионы переходят в карбонатные, которые, реагируя с присутствующими в растворе катионами кальция, выпадают в осадок (при превыще-нии произведения растворимости ПРсасо,). Параллельно магний осаждается в виде гидроокиси магния. Процессы могут быть описаны следующими уравнениями: 2С02-ЬСа(ОН)2 = Са(НСОз)2; Са(НСОз)2 4- Са(0Н)2 = 2СвСОз + 2Н2О; НСО3- + Са(0Н)2 = ОН- -Ь СаСОз + Н2О, Обычно одновременно с известкованием воды проводят и ее коагулирование. В качестве коагулянта, как правило, используют закисное сернокислое железо - железный купорос FeS04-7H20. 0 ... 108 109 110 111 112 113 114 ... 159 |
|||||||||||||||||||